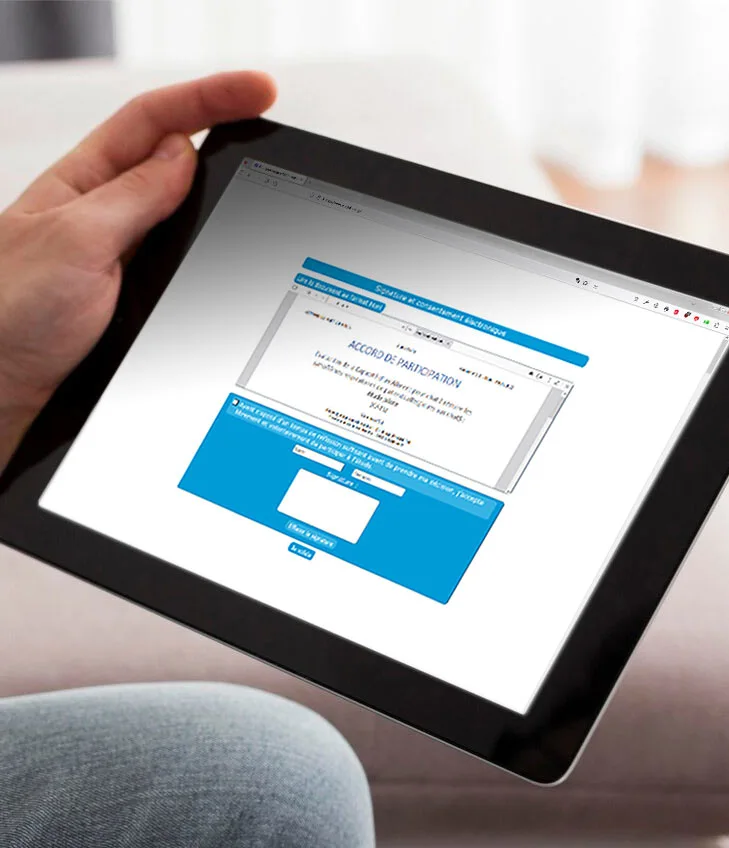
L’eConsent, ou consentement électronique, permet au médecin investigateur d’envoyer directement une demande de consentement via l’eCRF avant d’inclure son patient dans l’étude.
Seul ou intégré à l’eCRF, l’eConsent permet de simplifier le travail du moniteur tout en garantissant la sécurité et la confidentialité des données :
- Respect des procédures : impossibilité d’inclure un patient avant d’avoir signé,
- Simplicité : un code unique permet de relier le dossier du patient au consentement,
- Contrôle à distance : le moniteur peut suivre la procédure sans se déplacer au centree,
- Confidentialité : à distance, le moniteur n’a pas accès aux données nominatives,
- Sécurité : chiffrement des données nominatives ; protection des consentements par mot de passe,
- Traçabilité : un audit-trail complet de la procédure est imprimé sur chaque document.
La signature eConsent dans EOL est basée sur une signature dite « de niveau simple » selon eIDAS (règlement n° 910/2014/UE, adopté le 23 juillet 2014) et utilise le système OTP (One-Time Password).